2. 成都市食品药品检验研究院质量技术保障部, 四川 成都 610045;
3. 四川省医学科学院·四川省人民医院医院感染控制中心, 四川 成都 610072
2. Quality Technical Assurance Department, Chengdu Institute for Food and Drug Control, Chengdu 610045, China;
3. Center for Healthcare-associated Infection Control, Sichuan Academy of Medical Sciences and Sichuan Provincial People's Hospital, Chengdu 610072, China
腹膜炎是腹膜透析患者常见并发症。严重或长时间的腹膜炎会导致腹膜结构和功能的改变,最终导致腹膜透析失败,患者不得不改为长期血液透析治疗[1-3]。相关文献[4-7]报道,腹膜炎是导致腹膜透析患者死亡的主要原因之一,可占致死原因的16%。
2019年8月,某三级甲等综合医院医院感染管理部门通过该院腹膜透析中心监测信息发现,自该年6月以来,腹膜透析患者中腹膜炎发病人数明显增加,怀疑可能出现医院感染暴发。医院感染管理部门立即展开调查,以探索事件原因,制定干预措施。本文就此次调查、干预的过程和结果进行总结,报告如下。
1 资料与方法 1.1 调查对象某三级甲等综合医院肾脏疾病中心患者,该中心由1个血液透析中心、1个腹膜透析中心和2个住院病区组成。自2015年起腹膜透析中心建档的腹膜透析患者数超过300例。腹膜透析均为居家自行透析模式,患者定期至腹膜透析中心复诊,若出现腹膜炎等症状则收入病区治疗。本次调查在肾脏病病区和腹膜透析中心开展。
1.2 流行病学分析为了寻找并确认与此次事件相关的危险因素,采用病例对照研究和队列研究方法。
1.2.1 病例定义本调查中,使用国际腹膜透析协会(International Society for Peritoneal Dialysis,ISPD)腹膜透析相关性腹膜炎的诊断标准。当腹膜透析患者出现以下3项中至少2项时,可诊断为腹膜透析相关性腹膜炎[8]:(1)腹膜炎临床表现,即腹痛和/或透析液浑浊;(2)透出液白细胞计数>100/μL或>0.1×109/L(透析液至少在腹膜中停留2 h后再透出),且中性粒细胞>50%;(3)透出液细菌培养阳性。
1.2.2 调查工具文献报道,导致慢性衰竭的疾病、透析液污染、透析操作中的无菌技术以及胃肠道症状(如腹泻、便秘等)可能引发腹膜透析相关性腹膜炎[9]。访谈中医务人员认为患者在透析操作中的无菌技术(如手卫生、是否触碰腹膜透析导管口),摄入生冷食物而引起的肠胃不适以及患者家庭环境(如喂养宠物)可能与腹膜炎相关。患者访谈中,1例腹膜炎患者认为其使用的碘伏帽可能引起腹膜炎。基于上述信息制定此次调查表,收集有关危险因素,包括近期使用的碘伏帽品牌、腹膜透析液品牌、近期胃肠道症状(如腹泻、便秘等)、患者腹膜透析操作前手卫生、腹膜透析操作时是否佩戴口罩、腹膜透析操作时是否触碰腹膜透析导管口、是否重复使用碘伏帽、是否养宠物、操作过程中是否使用一次性治疗巾包裹导管口、近期是否进食生冷饮食、沐浴时是否污染透析导管口等。
1.2.3 病例对照研究采用1 ∶ 1配对病例对照研究。纳入2019年6月1日—8月17日符合病例定义的腹膜炎患者。如同一患者在此期间发生多次腹膜炎,则分别调查每次腹膜炎的相关情况,并均将其归入病例组。为每个病例匹配1例对照,对照为该期间未发生腹膜炎的腹膜透析患者,并排除性别、年龄、基础肾脏疾病对腹膜炎的影响,匹配标准为:(1)同性别、年龄差异<5岁、具有相同的肾脏基础疾病。(2)估计肾小球滤过率(eGFR)、残余肾功能指标(RRF)与病例同类别[<5 mL/(min·1.73 m2)或≥5 mL/(min·1.73 m2)][10]。
1.2.4 队列研究采用队列研究进一步确定危险因素以及该危险因素的存在时间。研究对象除了病例对照中的全部患者以外,还纳入2019年8月17日—9月30日腹膜透析中心接诊的所有腹膜透析患者。根据病例对照研究中发现的危险因素将患者分为两组,调查患者腹膜炎发生情况和危险因素存在日数。危险因素存在日数,对于发生腹膜炎的腹膜透析患者是从最近一批碘伏帽开始使用到发生腹膜炎的日数,对于未发生腹膜炎者则是从最近一批碘伏帽开始使用到调查当日的日数。
1.3 微生物学检测收集调查日(8月17日)所有腹膜透析相关性腹膜炎病例的透出液标本,进行细菌培养。收集上述病例未使用的同批次透析液和碘伏帽,进行细菌培养和内毒素检测。
1.4 统计学方法将所有数据输入Epi Data数据库(3.1.5版,美国疾病控制与预防中心),并使用SPSS 23.0软件(IBM公司)进行统计分析。病例对照研究计算比值比(OR)和95%可信区间(CI),在logistic回归分析中,采用后退逐步法,计算校正比值比(adjusted OR)、95%CI及P值,保留P≤0.05的变量。队列研究中,采用多因素Cox比例风险回归分析腹膜透析相关性腹膜炎的危险因素,使用Kaplan-Meier生存分析检验危险因素存在时间与发生腹膜炎的累积风险。P≤0.05为差异具有统计学意义。
2 结果 2.1 腹膜透析相关性腹膜炎发病情况2019年6—7月,腹膜透析中心的腹膜透析相关性腹膜炎的发病率分别为2.54%、3.99%,高于2015—2018年同期的平均发生率(1.18%和1.76%)。2019年8月开始停用“YW”牌碘伏帽后,腹膜透析相关性腹膜炎发生率下降至以往4年平均水平。见图 1。
 |
| 图 1 2019年和2015—2018年腹膜透析相关性腹膜炎发病情况 Figure 1 Occurrence of peritoneal dialysis-related peritonitis in 2019 and 2015-2018 |
腹膜透析患者通常居家自我透析,并常规周期性至腹膜透析中心进行复诊。当出现疑似腹膜炎症状时,患者立即至腹膜透析中心就诊,根据病情程度确定是否收入肾脏病病区住院治疗。2019年6月1日—8月17日,肾脏病病区收治19例腹膜透析患者,共发生24例次腹膜透析相关性腹膜炎。其中,1例患者在此期间发生3次腹膜炎,3例患者发生2次。19例患者的年龄为25~91岁,中位年龄为58岁;男性5例(26.32%),女性14例(73.68%);透析时间为1~58个月,中位时间为10.50个月。患者临床症状及实验室结果见表 1。
| 表 1 24例次腹膜透析相关性腹膜炎患者临床特征及实验室结果 Table 1 Clinical characteristics and laboratory results of 24 patients with peritoneal dialysis-related peritonitis |

|
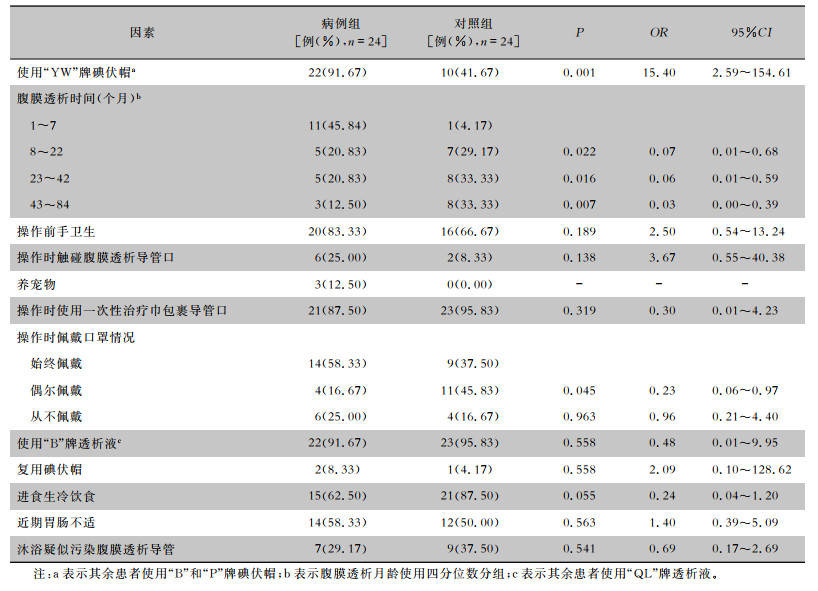
病例组纳入24例次腹膜透析相关性腹膜炎患者,对照组匹配24例患者。logistic回归分析表明,共有91.67%(22/24)的病例组患者使用“YW”牌碘伏帽,而对照组患者使用率仅为41.67%(10/24)。使用“YW”牌碘伏帽是腹膜透析相关性腹膜炎发生的独立危险因素(校正OR=15.40,95%CI:2.93~80.95,P=0.001)。见表 2。
| 表 2 腹膜透析相关性腹膜炎患者的危险因素分析 Table 2 Risk factors for patients with peritoneal dialysis-related peritonitis |
|
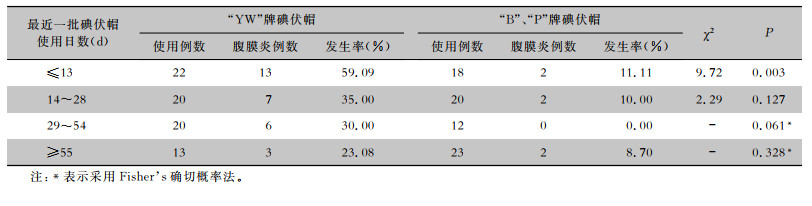
队列研究共纳入148例患者,根据碘伏帽的情况,将75例使用“YW”牌碘伏帽的患者纳入暴露组,73例使用“B”和“P”牌碘伏帽的患者纳入非暴露组。最近一批碘伏帽使用时间≤13 d时,使用“YW”牌碘伏帽患者的腹膜透析相关性腹膜炎的发生率高于使用“B”和“P”牌碘伏帽,差异有统计学意义(P<0.05),见表 3。Kaplan-Meier生存分析显示随着使用“YW”牌碘伏帽日数的增加,腹膜炎发生累积风险显著增加,见图 2。在多变量Cox比例风险回归分析中,同样显示使用“YW”牌碘伏帽是腹膜透析相关性腹膜炎发生的独立危险因素(HR=6.81,95%CI:2.61~17.77,P<0.01)。
| 表 3 两组患者碘伏帽不同使用日数的腹膜炎发生情况 Table 3 Occurrence of peritonitis in two groups of patients with different use days of iodophor cap |
|
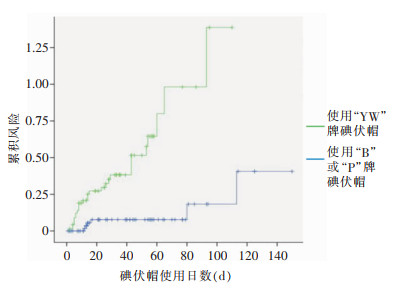 |
| 图 2 使用不同品牌碘伏帽的腹膜透析相关性腹膜炎累积风险图(Kaplan-Meier生存分析) Figure 2 Cumulative risk of peritoneal dialysis-related peritonitis using different brands of iodophor caps (Kaplan-Meier analysis) |
从腹膜透析相关性腹膜炎患者中共收集19袋腹膜透析液标本和19个碘伏帽(包括18个“YW”牌碘伏帽,1个“P”牌碘伏帽)进行细菌培养,均未见细菌生长;检测内毒素,结果均低于检测限。
3 讨论腹膜透析中心的监测数据显示,2015—2018年腹膜透析相关性腹膜炎的平均发病率为1%~2%。通常每年有两个发病高峰(2—3月和7—9月),可能与中国传统的春节和夏季饮食或生活习惯的变化有关。但即使在发病高峰,腹膜透析相关性腹膜炎发病率也不超过2%,而2019年6、7月份分别达到2.54%、3.99%,显著高于2015—2018年同期的平均发病率(1.18%和1.76%)。因此,2019年6、7月份该院可能存在腹膜透析相关性腹膜炎的暴发。
研究[11-12]报道,由于透析液的内毒素污染、腹膜内或腹腔脏器炎症反应、药物引起的化学性腹膜炎,会出现细菌培养结果阴性但透出液中中性粒细胞增多的情况。例如在患有胆囊炎、胰腺炎、阑尾炎、肾炎、疝或小肠嵌顿、持续非卧床腹膜透析并伴有肠系膜功能不全以及无菌性腹膜内脓肿破裂的病例中,存在中性粒细胞浸润到透析液中的情况[13-17]。另有腹膜透析液内毒素污染引起无菌性腹膜炎流行,腹腔内注入万古霉素或硫代硫酸钠注射液导致化学性腹膜炎的报道[18-20]。在本次调查中,腹膜炎患者未观察到腹膜内或腹腔脏器炎症反应,透析液的内毒素检测也排除了内毒素污染的可能性。
此次暴发的大多数病例与既往细菌性腹膜炎病例有显著不同。首先,仅有12.50%(3/24)的透出液培养结果显示细菌生长,而既往的腹膜炎患者透出液细菌培养结果阳性率高达70%~80%;其次,按照ISPD的建议,通过经验性使用抗菌药物来治疗腹膜炎[21-22],但是多例患者在治疗未中断的情况下发生多次腹膜炎(1例患者发生3次,3例患者发生2次),当实施干预措施后,上述患者很快完全治愈并出院;此外,流行病学调查显示,本次腹膜炎暴发“YW”牌碘伏帽引起,但是腹膜透析液和碘伏帽的内毒素检测和细菌培养结果均未发现细菌学证据。综合以上资料,判断为“YW”牌碘伏帽引起的腹膜透析相关性化学性腹膜炎暴发,推测可能是由“YW”牌碘伏帽中海绵上附着的化学物质引起。
当调查发现“YW”牌碘伏帽可引起腹膜透析相关性腹膜炎后,腹膜透析中心立即通知所有腹膜透析患者尤其是仍在住院治疗的腹膜炎患者停止使用“YW”牌碘伏帽。经此干预措施,腹膜透析相关性腹膜炎发病率很快降低到过去4年的平均水平。这一过程也进一步证实这是一起由“YW”牌碘伏帽引起的腹膜透析相关性化学性腹膜炎暴发。
本次调查存在的不足之处。首先,因检测技术限制,无法对碘伏帽中的化学物质进行分析,无法准确检出引起炎症反应的化学物质;其次,“YW”牌碘伏帽在全国腹膜透析患者中广泛使用,可能在许多开展腹膜透析治疗的医疗机构都出现了类似的腹膜炎患者,如果可以开展多中心调查,则相关影响因素的结论将更明确;此外,本次调查涉及多个批次“YW”牌碘伏帽,难以确定相关批号。
| [1] |
Ghali JR, Bannister KM, Brown FG, et al. Microbiology and outcomes of peritonitis in Australian peritoneal dialysis patients[J]. Perit Dial Int, 2011, 31(6): 651-662. DOI:10.3747/pdi.2010.00131 |
| [2] |
Lichodziejewska-Niemierko M, Chmielewski M, Wojtaszek E, et al. Current epidemiology and practice patterns in prevention and treatment of PD-related infections in Poland[J]. Int Urol Nephrol, 2019, 51(2): 335-341. DOI:10.1007/s11255-018-2057-9 |
| [3] |
Li M, Yan J, Zhang H, et al. Analysis of outcome and factors correlated with maintenance peritoneal dialysis[J]. J Int Med Res, 2019, 47(10): 4683-4690. DOI:10.1177/0300060519862091 |
| [4] |
Hamad A, Ismail H, Elsayed M, et al. The epidemiology of acute peritonitis in end-stage renal disease patients on peritoneal dialysis in Qatar: an 8-year follow-up study[J]. Saudi J Kidney Dis Transpl, 2018, 29(1): 88-94. DOI:10.4103/1319-2442.225203 |
| [5] |
Davenport A. Peritonitis remains the major clinical complication of peritoneal dialysis: the London, UK, peritonitis audit 2002-2003[J]. Perit Dial Int, 2009, 29(3): 297-302. DOI:10.1177/089686080902900314 |
| [6] |
Szeto CC, Wong TY, Chow KM, et al. Are peritoneal dialysis patients with and without residual renal function equivalent for survival study? Insight from a retrospective review of the cause of death[J]. Nephrol Dial Transplant, 2003, 18(5): 977-982. DOI:10.1093/ndt/gfg027 |
| [7] |
Auguste BL, Girsberger M, Kennedy C, et al. Are adverse events in newly trained home dialysis patients related to lear-ning styles? A single-centre retrospective study from Toronto, Canada[J]. BMJ Open, 2020, 10(1): e033315. DOI:10.1136/bmjopen-2019-033315 |
| [8] |
Li PKT, Szeto CC, Piraino B, et al. ISPD peritonitis recommendations: 2016 update on prevention and treatment[J]. Perit Dial Int, 2016, 36(5): 481-508. DOI:10.3747/pdi.2016.00078 |
| [9] |
Simões-Silva L, Araujo R, Pestana M, et al. Peritoneal microbiome in end-stage renal disease patients and the impact of peritoneal dialysis therapy[J]. Microorganisms, 2020, 8(2): 173. DOI:10.3390/microorganisms8020173 |
| [10] |
Kim HW, Kim SH, Kim YO, et al. The impact of timing of dialysis initiation on mortality in patients with peritoneal dialysis[J]. Perit Dial Int, 2015, 35(7): 703-711. DOI:10.3747/pdi.2013.00328 |
| [11] |
Rocklin MA, Teitelbaum I. Noninfectious causes of cloudy peritoneal dialysate[J]. Semin Dial, 2001, 14(1): 37-40. DOI:10.1046/j.1525-139x.2001.00012.x |
| [12] |
Steiner RW, Halasz NA. Abdominal catastrophes and other unusual events in continuous ambulatory peritoneal dialysis patients[J]. Am J Kidney Dis, 1990, 15(1): 1-7. DOI:10.1016/S0272-6386(12)80585-3 |
| [13] |
Prischl FC, Wallner M, Schauer W, et al. An important differential diagnosis in CAPD patients with sudden onset of fever, vomiting, abdominal pain, and cloudy dialysate[J]. Perit Dial Int, 1999, 19(1): 81-84. DOI:10.1177/089686089901900116 |
| [14] |
Cai BS, Thorp EB, Doran AC, et al. MerTK cleavage limits proresolving mediator biosynthesis and exacerbates tissue inflammation[J]. Proc Natl Acad Sci U S A, 2016, 113(23): 6526-6531. DOI:10.1073/pnas.1524292113 |
| [15] |
Streather CP, Carr P, Barton IK. Carcinoma of the kidney presenting as sterile peritonitis in a patient on continuous ambulatory peritoneal dialysis[J]. Nephron, 1991, 58(1): 121. DOI:10.1159/000186395 |
| [16] |
Syed A, Holley JL, Piraino B. Splenic infarct presenting as sterile peritonitis with peripheral embolic phenomena[J]. Adv Perit Dial, 1993, 9: 202-205. |
| [17] |
Bistrup C, Biegel E, Pedersen RS. Sterile peritonitis in a CAPD patient caused by a juxtaperitoneal abscess[J]. Nephrol Dial Transplant, 1995, 10(3): 406-407. |
| [18] |
Karanicolas S, Oreopoulos DG, Izatt S, et al. Epidemic of aseptic peritonitis caused by endotoxin during chronic peritoneal dialysis[J]. N Engl J Med, 1977, 296(23): 1336-1337. DOI:10.1056/NEJM197706092962309 |
| [19] |
Mangram AJ, Archibald LK, Hupert M, et al. Outbreak of sterile peritonitis among continuous cycling peritoneal dialysis patients[J]. Kidney Int, 1998, 54(4): 1367-1371. DOI:10.1046/j.1523-1755.1998.00110.x |
| [20] |
Charney DI, Gouge SF. Chemical peritonitis secondary to intraperitoneal vancomycin[J]. Am J Kidney Dis, 1991, 17(1): 76-79. DOI:10.1016/S0272-6386(12)80255-1 |
| [21] |
Campbell D, Mudge DW, Craig JC, et al. Antimicrobial agents for preventing peritonitis in peritoneal dialysis patients[J]. Cochrane Database Syst Rev, 2017, 4(4): CD004679. |
| [22] |
Morrisette T, Canada RB, Padgett D, et al. Factors associa-ted with increased hospital length of stay in peritoneal dialysis patients with peritonitis: a need for antimicrobial stewardship?[J]. Hosp Pharm, 2020, 55(1): 50-57. DOI:10.1177/0018578718817944 |



