2. 泰州市人民医院腔镜中心, 江苏 泰州 225300;
3. 泰州市人民医院临床检验中心, 江苏 泰州 225300
2. Endoscopy Center, Taizhou People's Hospital, Taizhou 225300, China;
3. Clinical Laboratory Center, Taizhou People's Hospital, Taizhou 225300, China
近年来,随着消化诊疗技术的不断发展,消化内镜(胃镜、肠镜、十二指肠镜等)的使用越来越广泛;另一方面,门诊内镜检查的患者越来越多,但检查前进行血源性传播疾病(HBV、HCV、HIV)筛查的难度较大,如果接触了血源性疾病患者的内镜清洗消毒不合格,极易造成患者的交叉感染甚至是血源性疾病的传播[1-2]。因此,消化内镜的清洗消毒质量已成为预防和控制医院感染,保证医疗质量非常重要的环节。由于内镜本身的结构复杂、构造精细、材质特殊、管腔较多,加上内镜的传统手工清洗方法,人为影响因素较多,如果操作不规范,极易导致内镜的损坏,以及细菌不能彻底清除,从而造成使用后内镜的清洗消毒质量得不到保证。本研究探讨了消化内镜的传统手工清洗消毒方法与全自动内镜清洗消毒机两种方法对内镜清洗消毒质量的影响。
1 资料与方法 1.1 研究资料收集某院消化内镜中心的109条可正常使用的消化内镜(包括胃镜64条、肠镜40条、十二指肠镜5条),其中使用年限<1年的内镜57条,1~3年的内镜22条,≥3年的内镜30条。将内镜根据编号进行分组,分组时排除因内镜使用时间过长及内镜的类型对结果造成的影响。一组设为试验组,共55条,采用全自动内镜清洗消毒机(产自山东新华)进行清洗消毒;一组设为对照组,共54条,采用传统的手工清洗消毒方法(迈尔一体化清洗工作站)。收集标准:在对患者进行胃肠镜检查后,由固定的4名经培训合格后的洗镜工人按《软式内镜清洗消毒技术规范》(WS 507—2016)要求正常清洗消毒后备用的内镜(包括手工清洗消毒和全自动清洗消毒机清洗消毒)。
1.2 仪器与消毒剂全自动软式内镜清洗消毒机Rider-60B(山东新华),内镜酶洗液为鲁沃夫生物膜多酶清洗剂,内镜消毒剂为4 000 mg/L络合氯消毒剂(万金),中和剂为0.1%硫代硫酸钠,ATP荧光检测仪为Clean-TraceTM NGi型荧光检测仪(3M公司)。
1.3 方法 1.3.1 清洗消毒方法根据《软式内镜清洗消毒技术规范》(WS 507—2016)对内镜进行清洗消毒。
1.3.1.1 手工清洗消毒流程预处理(由跟台护士在1:270酶液中反复送气送水10 s,并用含酶纱布擦拭内镜表面及插入部)→测漏→手工清洗、酶洗5 min→漂洗3 min→消毒5 min、灭菌40 min→终末漂洗3 min→干燥。总时间为消毒18 min左右,灭菌43 min。
1.3.1.2 内镜清洗消毒机清洗消毒流程预处理(同手工清洗)→测漏→手工清洗、酶洗5 min→漂洗→根据内镜清洗消毒机标准程序进行清洗消毒(酶洗5 min→漂洗3 min→消毒5 min、灭菌40 min→终末漂洗3 min→干燥)。机洗的消毒程序运行时间18 min左右,灭菌程序运行时间为43 min。
1.3.2 检测方法根据《软式内镜清洗消毒技术规范》(WS 507—2016)对内镜进行清洗消毒效果监测。
1.3.2.1 内镜的清洗质量采用目测法结合ATP生物荧光检测法检测内镜的清洗质量,两种方法检查均合格即为合格,并计算内镜的清洗合格率。目测法主要是通过肉眼观察内镜的表面是否清洁,有无污渍。ATP生物荧光检测法:取出一体式的检测棒,分别对内镜的不同部位(内镜表面、阀门、管腔)进行采样。检测内镜表面或阀门时用检测棒进行均匀涂抹,插入到含荧光素酶的激活液中。内镜管腔则用10 mL无菌生理盐水进行腔道冲洗后全量收集。用专用采样棒采集水样,与激活液充分振摇后插入到检测仪中进行检测,记录读数。判定标准:≤200 RLU为合格。目测法和ATP生物荧光检测法其中有一项不合格,即为不合格。内镜清洗合格率计算:内镜清洗合格率=清洗质量合格的内镜数/监测内镜总数×100%。
1.3.2.2 倾注培养法采用倾注培养法检测内镜的染菌量。分别对内镜的不同部位(内镜表面、阀门、腔道)进行采样,其中内镜的外表面、阀门口采用含相应中和剂的棉签进行采样,内镜管腔采用50 mL含0.1%硫代硫酸钠中和剂的洗脱液进行冲洗,全量收集后送检。将洗脱液1.0 mL接种平皿,倾注15~20 mL营养琼脂,(36±6)℃培养48 h,计数菌落数。菌落总数(CFU/件)=菌落数(CFU/平皿)×50,消毒内镜的合格标准:菌落总数≤20 CFU/件。其中有一个部位不合格,即为不合格。内镜的消毒合格率计算:内镜消毒合格率=消毒质量合格内镜数/监测内镜总数×100%。
1.4 统计学方法应用SPSS 17.0统计软件进行统计学分析,计数资料采用χ2检验或Fisher’s确切概率法进行比较,以P≤0.05为差异具有统计学意义。
2 结果 2.1 两组内镜的基本情况试验组共55条内镜,使用年限分别为:<1年29条,1~3年11条,≥3年15条;消化内镜类型:胃镜32条,肠镜20条,十二指肠镜3条。对照组共54条内镜,使用年限分别为:<1年28条,1~3年11条,≥3年15条;消化内镜类型:胃镜32条,肠镜20条,十二指肠镜2条。两组内镜不同使用年限、不同内镜类型构成比较,差异均无统计学意义(均P>0.05)。
2.2 两种方法清洗质量比较试验组内镜清洗总合格率为94.55%,对照组内镜清洗总合格率为83.33%,两组比较差异无统计学意义(P>0.05)。其中试验组内镜阀门的清洗合格率高于对照组(96.36% vs 85.19%),差异有统计学意义(P<0.05),而内镜表面、内镜管腔清洗合格率比较,差异均无统计学意义(均P>0.05)。见表 1。
| 表 1 两组内镜清洗质量合格情况比较[%(条)] Table 1 Comparison in qualified result of endoscope clea-ning quality between two groups(%[No. of endoscopes]) |

|
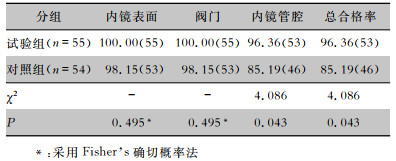
试验组内镜消毒总合格率为96.36%,对照组内镜消毒总合格率为85.19%,两组比较差异有统计学意义(P<0.05)。试验组内镜管腔消毒合格率高于对照组(96.36% vs 85.19%),差异有统计学意义(P<0.05),而两组内镜表面、阀门两个部位的消毒合格率比较,差异均无统计学意义(均P>0.05)。见表 2。
| 表 2 两组内镜消毒质量合格情况比较[%(条)] Table 2 Comparison in qualified result of endoscope disinfection quality between two groups(%[No. of endoscopes]) |
|
文献[3]报道内镜能够提供疾病诊断的信息,但同时也会因交叉污染给患者带来不必要的致命性的感染,因此,防控医院感染是内镜检查面临的重大问题。消化内镜结构比较复杂,管腔细长,并且有很多不易清洗的轴节、卡锁部位。研究[4]表明,使用后的消化内镜病原微生物载量可达105~1010 CFU/mL。因此,如何提高内镜的清洗消毒质量已成为预防和控制内镜感染的关键因素。
在本研究中,使用全自动清洗消毒机与手工清洗的合格率比较,差异无统计学意义,但对管腔的消毒效果优于手工清洗消毒。使用内镜全自动清洗消毒机进行清洗消毒具有操作简单方便、节省人力资源成本、减少消毒剂的暴露等优点,同时在整体清洗消毒流程上执行标准化操作流程(SOP),这样可大大降低人为因素对内镜清洗消毒效果的影响[5],同时也使工作人员免于长时间暴露于含消毒剂环境而产生的健康风险。
内镜的清洗环节是降低内镜表面污染的重要步骤,彻底清洗也是保证消毒效果的前提[6]。监测内镜清洗质量的主要方法是目测法、ATP生物荧光检测法。国内外研究[7-8]表明,ATP的含量与微生物的绝对数量以及血液浓度之间具有很强的关联性,ATP荧光检测法具有灵敏度高、重复性好的优点,极大地提高了检测效率和检测的准确性[9-10]。在研究中发现,如仅采用目测法检测内镜的清洗质量,只能发现极少量的不合格内镜,而使用ATP生物荧光检测内镜的清洗效果,无论全自动清洗消毒机还是传统的手工清洗消毒方法,在内镜的表面、阀门及管腔内均存在有检测不合格的现象,其检测清洗合格率为83.33%,也与国内的有关报道[11]基本一致。这些不合格内镜主要是集中在使用年限较长,特别是时间超过10年以上的内镜的关节、管腔部分,这与内镜由于频繁使用和清洗,并经消毒剂的长期浸泡,很多材质表面及管腔表面会出现凹凸不平甚至细微的肉眼不可见裂纹,而细菌和一些有机物如血液、黏液、组织会附着在这些缝隙、凹面以及难以清洗的内镜关节、卡锁部位,甚至会形成生物膜[12],这些会极大地影响内镜的清洗、消毒效果。而规范执行清洗操作,可有效去除内镜上生物污染物,有效防止生物膜的形成,提高内镜的清洗消毒效果[13]。但也有研究[14]表明,即使严格按照相关规范进行清洗消毒,仍会有生物膜不能完全清除,从而导致患者因行内镜检查而发生医院感染。因此,如果同一内镜多次监测不合格,且细菌培养结果为同一种细菌,经规范清洗消毒后监测仍不合格,则形成生物膜的可能性很大,建议返回原厂进行检测,专业去除生物膜,监测合格后方可再使用。
由于受条件所限,本研究中监测内镜消毒效果的方法采用的是倾注法,而在《医院消毒卫生标准》(GB 15982—2012)中对于内镜的消毒效果建议采用倾注法+滤膜法进行检测,且滤膜法的阳性率要高于倾注法和涂布法[15],因此对最终的结果可能会有一定的影响。但对于大多数医院,由于检测人员及设备的配备不足,滤膜法开展的可行性、可操作性不高,本研究将积极关注有无替代方法的最新研究进展。
综上所述,采用全自动清洗消毒机的消毒效果优于传统的手工清洗消毒。如部分医院因条件限制仍需采用传统的手工清洗消毒方法,则建议建立标准化的内镜清洗消毒流程,重点加强清洗消毒工作人员的培训,确保工作人员能够熟练掌握各项操作规范与流程,同时加强细节管理,强化监督与考核,确保措施的规范执行,最大限度地降低内镜诊疗引起医院感染的风险。
| [1] |
Noronha AM, Brozak S. A 21st century nosocomial issue with endoscopes[J]. BMJ, 2014, 348: g2047. DOI:10.1136/bmj.g2047 |
| [2] |
李少君, 马红录, 葛振宇. 消化内镜诊疗病人血源性传播疾病调查[J]. 中国消毒学杂志, 2013, 30(12): 1183-1184. |
| [3] |
Kovaleva J, Peters FT, van der Mei HC, et al. Transmission of infection by flexible gastrointestinal endoscopy and bronchoscopy[J]. Clin Microbiol Rev, 2013, 26(2): 231-254. DOI:10.1128/CMR.00085-12 |
| [4] |
Frăţilă O, Tanţău M. Cleaning and disinfection in gastrointestinal endoscopy:current status in Romania[J]. J Gastrointestin Liver Dis, 2006, 15(1): 89-93. |
| [5] |
柯萍, 袁璇, 陈晓冰. 标准化程序配合全自动内镜清洗消毒机在支气管纤维镜清洗消毒中的应用[J]. 广东医学, 2015, 36(8): 1306-1308. |
| [6] |
马久红, 胡雪飞, 刘林林, 等. 胃镜及肠镜预清洗的监测与评价[J]. 中华医院感染学杂志, 2012, 22(20): 4566-4567. |
| [7] |
Hammmes F, Goldschmidt F, Vital M, et al. Measurement and interpretation of microbial adenosine tri-phosphate(ATP) in aquatic environments[J]. Water Res, 2010, 44(13): 3915-3923. DOI:10.1016/j.watres.2010.04.015 |
| [8] |
黄昕, 李洁, 王志, 等. ATP含量与细菌数及血液稀释度的相关性研究[J]. 中华医院感染学杂志, 2012, 22(1): 15-17. |
| [9] |
赵奇, 刘吉起, 张玉勤, 等. ATP荧光检测法在卫生监测领域的应用[J]. 中国消毒学杂志, 2014, 31(2): 217-218. |
| [10] |
邹丽娟, 常后婵, 戴红霞, 等. 应用ATP荧光法监测腔镜器械清洗各环节的效果分析[J]. 护士进修杂志, 2012, 27(14): 1258-1260. DOI:10.3969/j.issn.1002-6975.2012.14.004 |
| [11] |
张骏骥, 李新芳, 乔美珍, 等. 苏州市医疗机构消化内镜清洗消毒现状调查[J]. 中国感染控制杂志, 2017, 16(7): 631-634. DOI:10.3969/j.issn.1671-9638.2017.07.009 |
| [12] |
周冬梅, 周岩岩, 卢玉文. 清洗环节质量控制对内镜管腔生物膜的影响[J]. 中国消毒学杂志, 2018, 35(2): 159-160. |
| [13] |
陆烨, 陆龙喜, 胡国庆, 等. 内镜管腔铜绿假单胞菌生物膜及其清洗效果的研究[J]. 中华医院感染学杂志, 2011, 21(14): 2970-2973. |
| [14] |
Hadi R, Vickery K, Deva A, et al. Biofilm removal by medical device cleaners:comparison of two bioreactor detection assays[J]. J Hosp Infect, 2010, 74(2): 160-167. DOI:10.1016/j.jhin.2009.10.023 |
| [15] |
朱艳秋, 张满, 杨怀, 等. 滤膜法与倾注法两种方法检测内镜消毒效果的结果比较[J]. 中国感染控制杂志, 2018, 17(6): 539-542. DOI:10.3969/j.issn.1671-9638.2018.06.016 |



