2. 中南大学湘雅医院医院感染控制中心, 湖南 长沙 410008;
3. 新药组合生物合成国家地方联合工程研究中心, 湖南 长沙 410205
2. Center for Healthcare-associated Infection Control, Xiangya Hospital, Central South University, Changsha 410008, China;
3. National Engineering Research Center of Combinatorial Biosynthesis for Drug Discovery, Changsha 410205, China
艰难梭菌(Clostridium difficile)是一种通过粪-口途径传播的革兰阳性厌氧芽孢杆菌,是导致胃肠炎相关感染的主要原因[1]。艰难梭菌芽孢在一般环境中可存活6个月,且耐热、耐酸,并对多种抗菌药物耐药。临床艰难梭菌感染(Clostridium difficile infection, CDI)可引起轻度腹泻至血样腹泻,严重感染患者可导致假膜性结肠炎、中毒性巨结肠、肠坏死,甚至危及生命。CDI的发病率不断增加[2],已经超过耐甲氧西林金黄色葡萄球菌(methicillin-resistant Staphylococcus aureus, MRSA),成为常见的医院感染病原体[3]。在社区和疗养院环境中,CDI也在增多[3-4]。CDI的高发病率、致死性和广泛的波及范围已引起医务人员的高度重视。预防和治疗CDI仍然是全球面临的公共卫生的重大挑战性问题之一。目前我国对CDI的认识不够充分,对艰难梭菌产毒株的检测能力和CDI的治疗方法有限。因此,了解CDI的严重程度和范围,将有助于医务人员进行诊断、预防和治疗。
1 CDI的致病过程艰难梭菌产毒株的毒力以及患者机体的免疫力是影响其感染的主要因素。人体肠道微生物在正常情况下,维持着良好的微生态平衡。然而,多种因素易破坏其平衡,包括广谱抗菌药物、抗肿瘤药物、免疫抑制剂等的使用,以及潜在的严重疾病及高龄因素。这些均可导致患者肠道内较为敏感的细菌丧失,而相对比较耐药的艰难梭菌产毒株则在肠道内定植并释放毒素,包括毒素A(TcdA)和毒素B(TcdB),从而导致肠道细胞病变,并引起腹泻和结肠炎[5]。毒素A和B引起鸟嘌呤三磷酸酶的Rho家族成员(Rho GTPases)失活[3],导致结肠细胞死亡和肠屏障功能丧失,以及中性粒细胞性结肠炎。新的超毒力艰难梭菌的出现导致CDI大幅度增加,包括可表达二元毒素(CDT)的艰难梭菌菌株BI,NAP1和027[6]。CDI的致病过程见图 1。
 |
| 图 1 CDI的致病过程 |
艰难梭菌相关性腹泻(Clostridium difficile-associated diarrhea,CDAD)是指腹泻患者有3次或更多次稀便,并维持至少2 d;同时,艰难梭菌产生的毒素TcdA和/或TcdB的酶免疫分析结果为阳性;肠镜检查结果符合CDI的病理表现[7]。此诊断标准是根据CDI的症状和体征表现,并结合粪便中产毒艰难梭菌的微生物学证据以及假膜性结肠炎(pseudomembranous colitis)的结肠镜检查或组织病理学表现,有效排除其他原因导致的假膜性结肠炎[8]。其中微生物学证据价值较大,粪便中的毒素检测是非常重要的环节。毒素检测方法包括艰难梭菌产毒素培养(toxinogenic culture)、细胞毒性中和试验(cell cytotoxicity neutralization assay, CCNA)、毒素酶免疫分析(enzyme immunoassay, EIA)、核酸扩增试验(nucleic acid amplification test, NAAT)以及毒素基因的聚合酶链反应(polymerase chain reaction, PCR)[9]。另外,谷氨酸脱氢酶(glutamate dehydrogenase, GDH)的酶免疫分析也可用于诊断。在这些方法中,艰难梭菌产毒素培养或细胞毒性中和试验被认为是过去30年诊断CDI的金标准。
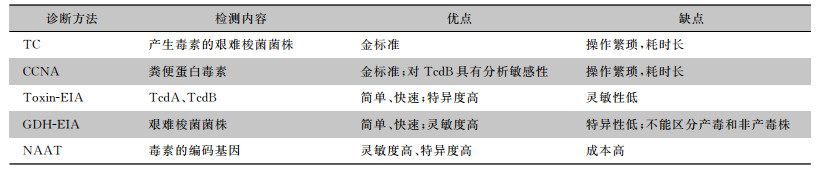
这些检测有其各自的特点,艰难梭菌产毒素培养检测艰难梭菌菌株的产毒素能力,如生物体检测,而细胞毒性中和试验直接检测粪便中的艰难梭菌毒素,细胞毒性中和试验对TcdB具有分析敏感性,TcdB历来被认为是临床疾病的良好标志物[6]。由于4%的健康成人有艰难梭菌定植,其中20%~25%的艰难梭菌菌株可能是非产毒株,因此,单纯的艰难梭菌实验室检测和鉴定不能诊断CDI。从培养毒素检测阳性中获得的艰难梭菌应使用细胞毒性中和试验和/或毒素酶免疫分析进行产毒情况评价,或使用核酸扩增试验进行TcdA或TcdB基因检测[10]。核酸扩增试验被认为是检测毒素基因的最具成本效益的方法,大多数核酸扩增试验检测靶向毒素TcdA、TcdB和/或二元毒素CDT的编码基因[11-12]。虽然核酸扩增试验方法被认为优于其他诊断方法,但这种检测策略不能准确区分艰难梭菌定植和感染,有时会导致过度诊断。过度诊断可能导致过度治疗CDI,延误对腹泻疾病及其暴发的其他原因的识别。这也导致不必要地使用抗菌药物,以及过高估计医院CDI的发病率[13]。虽然谷氨酸脱氢酶酶免疫分析方法筛选艰难梭菌敏感并且还显示出有利的阴性预测值,但这些方法不能区分产毒和非产毒菌株,因为两种菌株均产生谷氨酸脱氢酶。此外,谷氨酸脱氢酶酶免疫分析对艰难梭菌不是特异性的,与其他梭菌产生的类似酶存在交叉反应。GDH的酶免疫分析对艰难梭菌筛选试验的敏感性低于NAAT。在2009年,试剂盒C. Diff Quik Chek Complete可以同时检测谷氨酸脱氢酶和毒素TcdA/TcdB。该组合测试提供了一种快速、经济、简便的方法。该方法具有98%的特异性,而且检测结果可在30 min内完成,并可同时排除使用谷氨酸脱氢酶酶免疫分析的阴性结果,而无需进行额外的测试[6]。由于艰难梭菌的PCR检测反应是一种非常敏感的方法,且无法区分定植的患者,因此,在低风险患者中频繁使用PCR检测可能导致CDI的误诊。不应对感染概率低的患者(即没有风险因素且呕吐为主诉的患者)进行高敏感的PCR检测。此外,使用逆转录PCR(reverse transcription-PCR,RT-PCR)定量粪便样品中的艰难梭菌浓度,将有助于区分CDI患者和因其他原因导致腹泻的艰难梭菌定植患者。在临床实践中,对于腹泻患者,无论是酶免疫分析还是PCR检测结果阳性,都应及时治疗[3]。CDI实验室诊断方法的比较见表 1。
| 表 1 CDI实验室诊断方法的比较 |
|
对于艰难梭菌引起的感染,治疗方法多种多样,抗菌治疗仍然是CDI的首选,但目前可用的抗菌药物类别相对较少。再加上目前抗菌治疗的缺陷,包括治疗失败、耐万古霉素肠球菌(vancomycin-resistant enterococcus, VRE)出现、高复发率和高成本,开发新的抗菌药物迫在眉睫。非达霉素是一种窄谱大环内酯类抗生素,2011年被批准用于CDI的治疗[14]。目前正在研究其他针对艰难梭菌的窄谱抗菌药物[15],这些药物处于临床试验的不同阶段。此外,还出现了一些替代治疗策略和新策略,包括粪便移植。
3.1 用于CDI治疗的抗菌药物目前推荐用于治疗CDI的抗菌药物包括甲硝唑和万古霉素。虽然这两种抗菌药物均已使用了30多年,但仍然是首选治疗药物[16]。与万古霉素治疗比较,甲硝唑治疗失败率和复发率更高,尤其是对于重症患者[2, 17]。甲硝唑在重症患者中表现较差的潜在机制是:甲硝唑通过发生炎症的结肠黏膜在血流中输送,并且随着疾病的好转,粪便中艰难梭菌的浓度降低。由于重症患者结肠血流量减少,因此甲硝唑向黏膜和结肠腔的输送减少。当万古霉素作为初始治疗药物治疗CDI时,并发症的发生率较低[18]。然而,万古霉素治疗费用比甲硝唑更昂贵,且万古霉素的使用有可能增加万古霉素耐药菌的流行。口服甲硝唑的生物利用度较低,导致其体内药物浓度较低[19]。由于仅少量甲硝唑到达结肠,这也是药物治疗黏膜或腔内感染的药效学方面的缺点。此外,甲硝唑还具有全身性副作用,如恶心、头痛、味觉异常和周围神经病变。
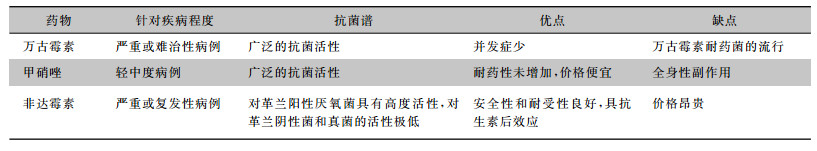
非达霉素对临床分离艰难梭菌的体外活性比万古霉素约高8倍[20]。非达霉素的这种活性,加上最低的全身吸收,高粪便浓度,以及体内体外对正常肠道菌群成分的活性有限等优点,于2011年上市[21]。CDI治疗的最大挑战是其高复发率。在用甲硝唑或万古霉素初始治疗成功后,20%~30%的患者在60 d内复发,但较多的患者通常在两周内复发[22]。疾病复发对患者构成重大负担,降低了生活质量,并增加发病率和病死率[23]。非达霉素治疗复发率较低,这一发现可能是由于在感染治疗期间肠道微生物组受损较小[22]。非达霉素对革兰阳性厌氧菌具有高度活性,但对革兰阴性菌和真菌的活性可忽略不计。相反,万古霉素和甲硝唑具有更广泛的抗菌活性[23]。非达霉素迅速杀死艰难梭菌,而万古霉素抑制其生长。总之,非达霉素和万古霉素在治疗CDI引起的急性腹泻病方面具有相似的效果,但非达霉素可以实现更持久的疾病消退。但非达霉素价格过高,限制了其临床使用[24],因此开发新的CDAD治疗方法至关重要,这些治疗方法应尽可能避免破坏肠道微生物群及促进与医疗保健相关病原体的过度生长[25]。目前用于CDI治疗的抗菌药物的比较见表 2。
| 表 2 目前用于艰难梭菌治疗的抗菌药物的比较 |
|
多个临床试验评估了CDI的多种抗菌药物,包括苏托霉素(CB-183, 315)、利地尼唑、LFF571、硝唑尼特、卡达唑胺和利福昔明等[15]。两种特殊类型的抗菌药物,包括恶唑烷和苏托霉素,均已完成临床Ⅲ期研究。另外两种抗菌药物,LFF571和利地尼唑,已经完成Ⅱ期研究。抗菌药物CRS3123正在进行Ⅰ期研究[26]。苏托霉素是一种环状脂肽,可通过口服给药,并选择性的杀死艰难梭菌[27]。其作用机制是通过破坏艰难梭菌细胞膜活性。苏托霉素由于缺乏对革兰阴性厌氧菌和兼性厌氧菌的活性,对正常胃肠道微生物群的干扰极小,这一特征与其复发率降低和临床治愈率较高有关[28]。因此,苏托霉素治疗CDI获得了比万古霉素更高的持续治愈率,以及较低的CDI复发率[27]。替加环素也被认为可作为标准治疗难治性CDI发作的合理补充,但仍然需要更多的临床药效证明[29]。卡达唑胺是一种新型恶唑烷酮杂合物,对艰难梭菌具有很强的抗菌活性,诱导抗性的倾向较低[30]。此外,在致毒艰难梭菌固定相培养中,卡达唑胺显著抑制TcdA和TcdB的形成,并且在生长抑制浓度下显著抑制艰难梭菌芽孢的形成[6]。咪唑烷具有与万古霉素相似的活性,可以完全保护仓鼠和小鼠模型免受由艰难梭菌引起的腹泻和死亡。LFF571是一种新型半合成硫肽,是革兰阳性菌的有效抑制剂。LFF571的抑菌活性是通过抑制艰难梭菌蛋白合成实现的,通过与延伸因子Tu(EF-Tu)相互作用,并中断EF-Tu和氨酰-tRNA之间的复合物形成来抑制艰难梭菌蛋白质合成[31]。该化合物在CDI仓鼠模型中比万古霉素更有效,其有效剂量及复发率均更低[32]。利地尼唑是一种新型、窄谱、不可吸收的小分子抗菌药物,对艰难梭菌具有较好的活性,可显著降低毒素的产生并减轻炎症反应[33]。然而,这种药物的具体作用机制仍不清楚,该药物似乎不通过常见抗菌机制起作用,例如抑制细胞壁、蛋白质、脂质、RNA或DNA合成[20]。在荧光标记研究中,当抗菌药物浓度低于利地尼唑的最低抑制浓度时,艰难梭菌的治疗结果为丝状表型,这意味着利地尼唑可能损伤细胞分裂。血浆中利地尼唑水平低于检测限,说明肠道对利地尼唑的吸收较低。此结果证明了利地尼唑的不可吸收性和低全身暴露。这种对肠道微生物群无附带损伤的情况可能会降低CDI的复发率。
CDI的理想治疗方法是在保留原肠道菌群完整的情况下,以艰难梭菌为靶点,从而恢复治疗过程中的菌落耐药性和健康菌群[20]。CRS3123是一种小分子窄谱剂,具有革兰阳性覆盖和有限的口服生物利用度,其使用导致胃肠道中的高浓度药物和低全身暴露。该试剂是一种新型的氨酰-tRNA合成酶抑制剂,这种独特的抗菌药物在抑制艰难梭菌的生长、芽孢形成和毒素生成中起作用。有机硒化合物依布硒啉可通过化学合成,可直接作用于艰难梭菌毒素的葡萄糖基转移酶结构域,依布硒啉对TcdA和TcdB均有较好的抑制作用,在与人类感染相似的小鼠模型的治疗试验中,依布硒啉通过抑制葡萄糖基转移酶,降低了小鼠组织的疾病病理表现[34]。托勒伐(tolevamer)是一种口服给药的毒素结合聚合物[15],可能吸收CDI中涉及的毒素,与甲硝唑和万古霉素治疗比较,中止腹泻的时间和临床成功率较低。然而,这些阴离子结合树脂可能仍然用作抗菌药物的替代物,作为治疗CDI的新兴替代物[35]。
3.3 单克隆抗体和疫苗艰难梭菌毒素的表达是CDI发生的必要条件,因此,开发单克隆抗体等药物防止毒素的细胞毒性作用是一种合理的控制疾病的策略[6]。Bezlotoxumab (MK-6072)是一种人类单克隆抗体。该抗体通过阻断艰难梭菌TcdB与宿主细胞的结合,从而降低肠道表皮细胞损伤,促进微生物群落恢复,从而减少复发性CDI[8]。默沙东公司还开发了另一种人类单克隆抗体actoxumab (MK-3415),用于中和艰难梭菌毒素A75[8]。CDI患者中的IgG具有一定的抗毒素能力,意味着CDI疫苗也可预防CDI[15]。虽然目前还没有针对CDI的有效疫苗,但有三种艰难梭菌疫苗处于不同的临床试验阶段。CDI Cffense (NCT01887912)是一种由赛诺菲巴斯德生产[6]的含有TcdA和TcdB类毒素的疫苗。IC84 (NCT02316470)是两种毒素TcdA和TcdB的重组蛋白组成的疫苗,以及辉瑞公司正在开发的一种双价毒素疫苗(NCT02561195,NCT02117570)。上述候选疫苗都以TcdA和TcdB为靶标。其他在研制的疫苗包括基于多糖聚糖的重组疫苗、糖偶联疫苗和基于DNA的疫苗[36]。但是,由于疫苗接种和单克隆抗体的使用都不可能消除艰难梭菌的感染和定植,因此仍然需要隔离艰难梭菌患者以防止其传播。
3.4 粪便菌群移植和益生菌疗法粪便菌群移植(fecal microbiota transplantation, FMT)是指将健康供体的粪便悬浮液输注于受者体内,旨在恢复CDI患者的正常肠道微生物群,达到治疗CDI的目的。从本质上讲,粪便菌群移植的作用是在患者结肠内重建多样的、正常的肠道微生物群,打破CDI的复发循环。该方法已经使用一千多年,但自2010年以来开始被认为是治疗复发性CDI的有效方法,相对于抗菌治疗的优势受到广泛赞誉[37]。然而,粪便菌群移植在治疗CDI中的作用机制仍不清楚,但是拟杆菌和厚壁菌是需要移植材料的关键成分[15]。2019年2月Mullish等[36]研究发现,粪便菌群移植可能通过恢复肠道菌群的胆盐水解酶活性,以促进牛磺胆酸的水解,从而治疗复发性CDI[38]。粪便菌群移植中培养的粪便细菌替代粪便正在试验中。口服含有粪便细菌芽孢的胶囊已经显示出治疗复发性疾病的功效[15]。总之,当传统抗菌药物治疗无效时,粪便菌群移植被认为是一种简单、可接受的CDI治疗方法。尽管粪便菌群移植仍存在许多挑战,但将其广泛用于治疗难治性或复发性CDI有一定的治疗前景[24]。
益生菌治疗是恢复结肠微生物群的另一种策略。益生菌含有单一培养或混合培养的活微生物,如细菌或酵母。益生菌治疗CDI的作用机制包括通过抑制黏附、调节宿主反应和刺激特异性IgA抗毒素的产生而直接对艰难梭菌产生活性[9]。除了粪便菌群移植和益生菌治疗外,还应考虑尽量减少对正常肠道微生物群落的破坏。一些抗菌肽如苏云金菌素、乳链菌肽和乳酸3147已证明对艰难梭菌和其他革兰阳性菌有选择性和有效的抑制作用,而且对其他共生肠道微生物影响较小[36]。非产毒艰难梭菌菌株的使用也是另一种防止产毒性艰难梭菌定植肠道的方法。与粪便菌群移植非常相似,此策略的使用是通过产生非毒素的艰难梭菌定植胃肠道,从而防止产生毒素菌株的定植[39]。另外,噬菌体溶素蛋白也可用于治疗CDI。从艰难梭菌CD630基因组的噬菌体裂解蛋白序列中可克隆出一种噬菌体裂解蛋白及其催化结构域(PlyCD1-174),证明其具有良好的裂解艰难梭菌的能力。此外,人类α-防御素HNP-1、HNP-3和HD-5在预防艰难梭菌毒素B对肠上皮细胞和大量其他细胞的细胞毒性作用方面也有潜在的作用[38]。
4 展望本文讨论了关于CDI诊断和治疗的近期研究进展。CDI诊断和治疗的现状仍然存在较多挑战。由于抗菌药物的使用是CDI的最主要危险因素,抗菌药物管理是预防和控制CDI的必要条件。实施抗菌药物管理计划,应尽量减少抗菌药物治疗的频率和持续时间,并限制使用与CDI相关的抗菌药物,如头孢菌素和克林霉素,以降低其风险[11]。另外,由于艰难梭菌通常存在于医疗机构中,因此,应实施旨在预防该疾病在医院中传播的措施,以医院为基础的感染控制程序可以帮助减少CDI的发病率[11]。环境清洁和消毒对于阻断艰难梭菌的传播和降低CDI的发病率也很重要。
快速准确的诊断是预防和控制CDI的关键步骤,可以选用多种诊断方法。在CDI的治疗方面,现有的治疗药物和有效的疫苗仍然有限。抗菌药物治疗仍然是CDI的首选,同时应考虑其他治疗策略,如粪便菌群移植和外科手术干预。在选择抗菌药物的处方药物发生变化后监测CDI的发病率也是必要的[6]。在合理使用目前现有抗菌药物的同时,开发针对CDI的新型抗菌药物值得期待。
致谢: 感谢段燕文教授对本文写作和修改过程中给予的建设性意见!
| [1] |
Hall AJ, Curns AT, McDonald LC, et al. The roles of Clostridium difficile and norovirus among gastroenteritis-associa-ted deaths in the United States, 1999-2007[J]. Clin Infect Dis, 2012, 55(2): 216-223. DOI:10.1093/cid/cis386 |
| [2] |
Zar FA, Bakkanagari SR, Moorthi KM, et al. A comparison of vancomycin and metronidazole for the treatment of Clostri-dium difficile-associated diarrhea, stratified by disease severity[J]. Clin Infect Dis, 2007, 45(3): 302-307. DOI:10.1086/519265 |
| [3] |
Lessa FC, Mu Y, Bamberg WM, et al. Burden of Clostridium difficile infection in the United States[J]. N Engl J Med, 2015, 372(9): 825-834. DOI:10.1056/NEJMoa1408913 |
| [4] |
李贞, 章黎华, 董丹凤, 等. 艰难梭菌感染的流行状况及耐药机制研究进展[J]. 上海交通大学学报(医学版), 2014, 34(6): 919-923. |
| [5] |
李春辉.艰难梭菌多位点序列分型及感染危险因素的流行病学[D].长沙: 中南大学, 2014.
|
| [6] |
Peng Z, Ling L, Stratton CW, et al. Advances in the diagnosis and treatment of Clostridium difficile infections[J]. Emerg Microbes Infect, 2018, 7(1): 15. |
| [7] |
Larrainzar-Coghen T, Rodriguez-Pardo D, Puig-Asensio M, et al. First recurrence of Clostridium difficile, infection:clinical relevance, risk factors, and prognosis[J]. Eur J Clin Microbiol Infect Dis, 2016, 35(3): 371-378. DOI:10.1007/s10096-015-2549-9 |
| [8] |
Ofosu A. Clostridium difficile infection:a review of current and emerging therapies[J]. Ann Gastroenterol, 2016, 29(2): 147-154. |
| [9] |
Carroll KC, Bartlett JG. Biology of Clostridium difficile:implications for epidemiology and diagnosis[J]. Annu Rev Microbiol, 2010, 65(1): 501-521. |
| [10] |
Crobach MJ, Planche T, Eckert C, et al. European Society of Clinical Microbiology and Infectious Diseases:update of the diagnostic guidance document for Clostridium difficile infection[J]. Clin Microbiol Infect, 2016, 22(Suppl 4): S63-S81. |
| [11] |
Surawicz CM, Brandt LJ, Binion DG, et al. Guidelines for dia-gnosis, treatment, and prevention of Clostridium difficile infections[J]. Am J Gastroenterol, 2013, 108(4): 478-498. DOI:10.1038/ajg.2013.4 |
| [12] |
中国医师协会检验医师分会感染性疾病检验医学专家委员会. 中国成人艰难梭菌感染诊断和治疗专家共识[J]. 协和医学杂志, 2017, 8(3): 131-138. |
| [13] |
Polage CR, Gyorke CE, Kennedy MA, et al. Overdiagnosis of Clostridium difficile infection in the molecular test era[J]. JAMA Intern Med, 2015, 175(11): 1792-1801. DOI:10.1001/jamainternmed.2015.4114 |
| [14] |
Reigadas E, Alcalá L, Marín M, et al. In vitro activity of surotomycin against contemporary clinical isolates of toxigenic Clostridium difficile strains obtained in Spain[J]. J Antimicrob Chemother, 2015, 70(8): 2311-2315. DOI:10.1093/jac/dkv092 |
| [15] |
Beinortas T, Burr NE, Wilcox MH, et al. Comparative efficacy of treatments for Clostridium difficile infection:a syste-matic review and network meta-analysis[J]. Lancet Infect Dis, 2018, 18(9): 1035-1044. DOI:10.1016/S1473-3099(18)30285-8 |
| [16] |
Debast SB, Bauer MP, Kuijper EJ. European Society of Clinical Microbiology and Infectious Diseases:update of the treatment guidance document for Clostridium difficile infection[J]. Clin Microbiol Infect, 2014, 20(Suppl 2): 1-26. |
| [17] |
Bartlett JG. The case for vancomycin as the preferred drug for treatment of Clostridium difficile infection[J]. Clin Infect Dis, 2008, 46(10): 1489-1492. DOI:10.1086/589465 |
| [18] |
Gerding DN, File JT, McDonald LC. Diagnosis and treatment of Clostridium difficile infection (CDI)[J]. Infect Dis Clin Pract, 2016, 24(1): 3-10. DOI:10.1097/IPC.0000000000000350 |
| [19] |
Vickers RJ, Tillotson G, Goldstein EJ, et al. Ridinilazole:a novel therapy for Clostridium difficile infection[J]. Int J Antimicrob Agents, 2016, 48(2): 137-143. DOI:10.1016/j.ijantimicag.2016.04.026 |
| [20] |
Karlowsky JA, Laing NM, Zhanel GG. In vitro activity of OPT-80 tested against clinical isolates of toxin-producing Clostridium difficile[J]. Antimicrob Agents Chemother, 2008, 52(11): 4163-4165. DOI:10.1128/AAC.00476-08 |
| [21] |
丁百兴, 王明贵. 非达霉素:一种治疗艰难梭菌感染的新选择[J]. 中国感染与化疗杂志, 2014, 14(6): 534. DOI:10.3969/j.issn.1009-7708.2014.06.015 |
| [22] |
Louie TJ, Miller MA, Mullane KM, et al. Fidaxomicin versus vancomycin for Clostridium difficile Infection[J]. N Engl J Med, 2011, 364(5): 422-431. DOI:10.1056/NEJMoa0910812 |
| [23] |
Cornely OA, Miller MA, Louie TJ, et al. Treatment of first recurrence of Clostridium difficile infection:fidaxomicin versus vancomycin[J]. Clin Infect Dis, 2012, 55(Suppl 2): S154-S161. DOI:10.1093/cid/cis462 |
| [24] |
Bang BW, Park JS, Kim HK, et al. Fecal microbiota transplantation for refractory and recurrent Clostridium difficile infection:a case series of nine patients[J]. Korean J Gastroenterol, 2017, 69(4): 226-231. DOI:10.4166/kjg.2017.69.4.226 |
| [25] |
Al-Nassir WN, Sethi AK, Li Y, et al. Both oral metroni-dazole and oral vancomycin promote persistent overgrowth of vancomycin-resistant Enterococci during treatment of Clostri-dium difficile-associated disease[J]. Antimicrob Agents Chemother, 2008, 52(7): 2403-2406. DOI:10.1128/AAC.00090-08 |
| [26] |
Fehér C, Soriano A, Mensa J. A review of experimental and off-label therapies for Clostridium difficile infection[J]. Infect Dis Ther, 2017, 6(1): 1-35. DOI:10.1007/s40121-016-0140-z |
| [27] |
Mascio CTM, Chesnel L, Thorne G, et al. Surotomycin de-monstrates low in vitro frequency of resistance and rapid bactericidal activity in Clostridium difficile, Enterococcus faecalis, and Enterococcus faecium[J]. Antimicrob Agents Chemother, 2014, 58(7): 3976-3982. DOI:10.1128/AAC.00124-14 |
| [28] |
Chilton CH, Crowther GS, Todhunter SL, et al. Efficacy of surotomycin in an in vitro gut model of Clostridium difficile infection[J]. J Antimicrob Chemother, 2014, 69(9): 2426-2433. DOI:10.1093/jac/dku141 |
| [29] |
Kali A, Charles MV, Srirangaraj S. Cadazolid:a new hope in the treatment of Clostridium difficile infection[J]. Australas Med J, 2015, 8(8): 253-262. |
| [30] |
Leeds JA, Sachdeva M, Mullin S, et al. Mechanism of action of and mechanism of reduced susceptibility to the novel anti-Clostridium difficile compound LFF571[J]. Antimicrob Agents Chemother, 2012, 56(8): 4463-4465. DOI:10.1128/AAC.06354-11 |
| [31] |
Trzasko A, Leeds JA, Praestgaard J, et al. Efficacy of LFF571 in a hamster model of Clostridium difficile infection[J]. Antimicrob Agents Chemother, 2012, 56(8): 4459-4462. DOI:10.1128/AAC.06355-11 |
| [32] |
Goldstein EJ, Citron DM, Tyrrell KL. Comparative in vitro activities of SMT19969, a new antimicrobial agent, against 162 strains from 35 less frequently recovered intestinal Clostridium species:implications for Clostridium difficile recurrence[J]. Antimicrob Agents Chemother, 2014, 58(2): 1187-1191. DOI:10.1128/AAC.02184-13 |
| [33] |
Bender KO, Garland M, Ferreyra JA, et al. A small-molecule antivirulence agent for treating Clostridium difficile infection[J]. Sci Transl Med, 2015, 7(306): 306r. |
| [34] |
Johnson S, Louie TJ, Gerding DN, et al. Vancomycin, metro-nidazole, or tolevamer for Clostridium difficile infection:results from two multinational, randomized, controlled trials[J]. Clin Infect Dis, 2014, 59(3): 345-354. DOI:10.1093/cid/ciu313 |
| [35] |
Wilcox M, Gerding D, Poxton I, et al. Bezlotoxumab alone and with actoxumab for prevention of recurrent Clostridium difficile infection in patients on standard of care antibiotics:integrated results of 2 phase 3 studies (MODIFY I and MODIFY II)[J]. Open Forum Infect Dis, 2015, 2: 67. DOI:10.1093/ofid/ofv131.06 |
| [36] |
Mullish BH, McDonald JAK, Pechlivanis A, et al. Microbial bile salt hydrolases mediate the efficacy of faecal microbiota transplant in the treatment of recurrent Clostridioides difficile infection[J]. Gut, 2019, pii:gutjnl-2018-317842. |
| [37] |
Gerding DN, Meyer T, Lee C, et al. Administration of spores of nontoxigenic Clostridium difficile strain M3 for prevention of recurrent C.difficile infection:a randomized clinical trial[J]. JAMA, 2015, 313(17): 1719-1727. DOI:10.1001/jama.2015.3725 |
| [38] |
Wang Q, Euler CW, Delaune A, et al. Using a novel lysin to help control Clostridium difficile infections[J]. Antimicrob Agents Chemother, 2015, 59(12): 7447-7457. DOI:10.1128/AAC.01357-15 |
| [39] |
Giesemann T, Guttenberg G, Aktories K. Human alpha-defensins inhibit Clostridium difficile toxin B[J]. Gastroente-rology, 2008, 134(7): 2049-2058. DOI:10.1053/j.gastro.2008.03.008 |



