2. 襄阳市中心医院 湖北文理学院附属医院皮肤科, 湖北 襄阳 441021;
3. 襄阳市中心医院 湖北文理学院附属医院肾病内科, 湖北 襄阳 441021
2. Department of Dermatology, Xiangyang Central Hospital, Affiliated Hospital of Hubei University of Arts and Sciences, Xiangyang 441021, China;
3. Department of Nephropathy Internal Medicine, Xiangyang Central Hospital, Affiliated Hospital of Hubei University of Arts and Sciences, Xiangyang 441021, China
嗜麦芽窄食单胞菌(Stenotrophomonas maltophilia,SMA)是广泛存在于自然界的一种非发酵革兰阴性菌。中国细菌耐药监测网显示,2016年我国SMA分离率在非发酵菌中仅次于铜绿假单胞菌和鲍曼不动杆菌[1]。2005—2017年陆军军医大学第一附属医院住院患者SMA分离率为2.9%,且呈逐年增加趋势[2]。SMA现已成为医院感染的主要条件致病菌之一,抵抗力低下及基础病较重的患者为其易感人群,呼吸道为其易感部位。此外,SMA对碳青霉烯类等广谱抗菌药物天然耐药,容易获得外源性耐药基因而致多重耐药[2],故临床治疗较为困难,严重影响患者的预后。研究[3]报道,医院感染SMA患者的病死率可高达21%~69%。了解SMA医院感染的高危因素,及时有效的针对性治疗是提高其临床疗效,降低病死率的关键。目前,国内外关于医院感染SMA危险因素的报道很多,但存在纳入样本量少、危险因素指标不全面等缺陷,因此临床指导意义有限。本研究旨在通过Meta分析方法对医院感染SMA的危险因素进行系统评价,为临床治疗制定防控策略和降低SMA感染病死率等提供理论依据。
1 资料与方法 1.1 文献纳入及排除标准 1.1.1 纳入标准(1) 研究类型:病例对照研究,语种设定为中文和英文。(2)研究对象:根据是否感染SMA,分为感染组和非感染组。(3)诊断标准:有明确的SMA感染诊断方法及标准。(4)感染组和非感染组有明确的暴露因素,且纳入文献至少包含1个危险因素。
1.1.2 排除标准(1) 病例报道、社论、综述和基础性研究;(2)数据不全且无法通过其他途径获得;(3)文献质量过低[纽卡斯尔-渥太华量表(Newcastle-Ottawa Scale,NOS)评分≤ 3分];(4)重复发表或研究对象有重叠的文献;(5)无法获取危险因素的OR值及95%CI的文献。
1.2 文献检索策略检索PubMed、Embase、Cochrane Library、中国期刊全文数据库(CNKI)、中国生物医学文献数据库(CBM)、万方数据库以及维普数据库(VIP)中有关医院感染SMA危险因素的病例对照研究,检索时间为从建库至2019年3月。中文检索词:嗜麦芽窄食单胞菌、医院感染、医院获得性感染、医疗保健相关感染、真菌感染、危险因素、影响因素、相关因素;英文检索词:Stenotrophomonas maltophilia,SMA,nosocomial infection,hospital infection,risk factor。检索策略为:(Stenotropho-monas maltophilia OR SMA)AND(nosocomial infection OR hospital infection OR hospital-acquired infection OR cross infection)AND (risk factor OR factor)。同时对相关内容的综述和纳入文献的参考文献进行手工检索,以发现潜在的、符合纳入标准的研究。
1.3 数据提取及质量评价由两名研究者独立按照文献纳入标准及排除标准筛选检索到的文献,提取的数据信息如下:第一作者姓名、发表时间、文献来源,纳入文献病例基本特征、SMA感染可能的危险因素。如两名研究者有不一致意见,双方讨论解决,仍有分歧,征求第三方意见。并根据NOS[4]对纳入文献质量进行评价,评价项目包括人群选择、可比性、暴露评价3个方面共8个条目对文献质量进行评价,满分为9分,7分及以上认为是高质量文献,4~6分为中等质量文献,1~3分为低质量文献。
1.4 统计学方法应用RevMan 5.3软件进行统计学分析。采用I2判断纳入文献的异质性,当P>0.1和I2 < 50%,采用固定效应模型;否则,应用随机效应模型。计数资料计算OR及其95%CI,计量资料则计算加权均数差(MD)及其95%CI,以P≤0.05为差异有统计学意义。敏感性分析采用同时计算固定效应模型和随机效应模型的OR值和95%CI,并比较两组结果。通过改变数据分析模型进行敏感性分析。若改变模型后无实质性改变(改变模型后不会得出相反的结论),说明合并结果较为稳定。根据漏斗图是否对称,评估有无发表偏倚,若对称,则提示可能无发表偏倚;若不对称,则提示可能存在发表偏倚。
2 结果 2.1 文献检索流程及结果初始检索到相关文献168篇,按照文献纳入标准及排除标准,通过阅读文题、摘要和全文后纳入10篇研究文献,3篇为英文文献,7篇为中文文献,文献筛选流程见图 1。
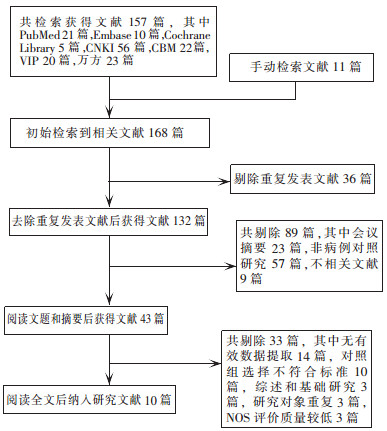 |
| 图 1 医院感染SMA危险因素Meta分析文献纳入及排除流程图 Figure 1 Flow chart of inclusion and exclusion of literatures for Meta-analysis on risk factors of SMA HAI |
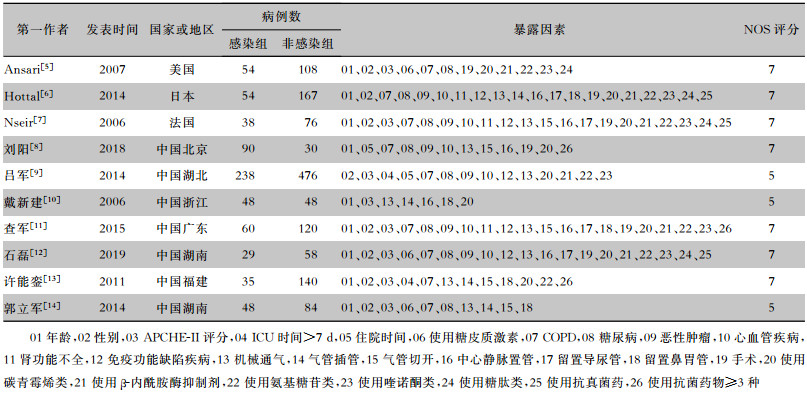
纳入的10篇文献均为病例对照研究,1篇文献[5]来自美国人群,1篇文献[6]来自日本,1篇文献[7]来自法国,7篇文献[8-14]的患者来自中国人群,共涉及2 001例患者,其中SMA感染组为694例,非感染组为1 307例,共提取出26种SMA感染的暴露因素。利用NOS对10篇纳入文献进行质量评估,7篇[5-8, 11-13]为7分,3篇[9-10, 14]为5分,均为优等文献,文献发表偏倚风险较低。纳入文献基本特征及质量评价见表 1。
| 表 1 医院感染SMA危险因素Meta分析纳入文献基本特征及质量评价 Table 1 Basic characteristics and quality evaluation of included literatures for Meta-analysis on risk factors of SMA HAI |
|
经异质性检验,年龄、性别、APCHE-Ⅱ评分、住院时间、使用糖皮质激素、糖尿病、恶性肿瘤、心血管疾病、肾功能不全、免疫功能缺陷性疾病、气管插管、切管切开、中心静脉置管、手术、使用碳青霉烯类、使用氨基糖苷类、使用抗菌药物≥3种等因素的异质性较好(P>0.10,I2 < 50%),采用固定效应模型进行效应量合并;APCHE-Ⅱ评分>20分、COPD、机械通气、留置导尿管、留置鼻胃管、使用β-内酰胺酶抑制剂、使用喹诺酮类、使用糖肽类和抗真菌药等因素存在异质性(P < 0.10,I2>50%),采用随机效应模型进行效应量合并。
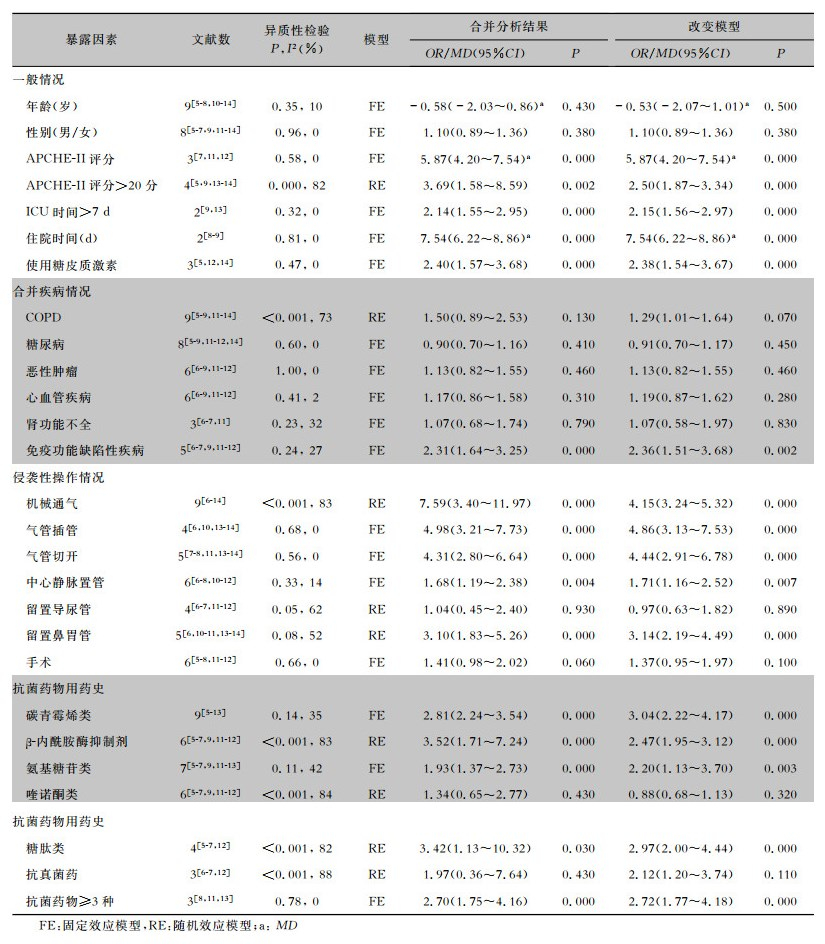
Meta分析结果显示,APCHE-Ⅱ评分(MD=5.87,95%CI:4.20~7.54)、APCHE-Ⅱ评分>20分(OR=3.69,95%CI:1.58~8.59)、住重症监护病房(ICU)时间>7 d(OR=2.14,95%CI:1.55~2.95)、住院时间(MD=7.54,95%CI:6.22~8.86)、使用糖皮质激素(OR=2.40,95%CI:1.57~3.68)、合并免疫功能缺陷性疾病(OR=2.31,95%CI:1.64~3.25)、机械通气(OR=7.59,95%CI:3.40~11.97)、气管插管(OR=4.98,95%CI:3.21~7.73)、气管切开(OR=4.31,95%CI:2.80~6.64)、中心静脉置管(OR=1.68,95%CI:1.19~2.38)、留置鼻胃管(OR=3.10,95%CI:1.83~5.26)、使用碳青霉烯类(OR=2.81,95%CI:2.24~3.54)、使用β-内酰胺酶抑制剂(OR=3.52,95%CI:1.71~7.24)、使用氨基糖苷类(OR=1.93,95%CI:1.37~2.73)、使用糖肽类(OR=3.42,95%CI:1.13~10.32)和使用抗菌药物≥3种(OR=2.70,95%CI:1.75~4.16)是医院感染SMA的危险因素,患者年龄、性别、合并COPD、合并糖尿病、合并恶性肿瘤、合并心血管疾病、合并肾功能不全、留置导尿管、手术、使用喹诺酮类和使用抗真菌药物与SMA感染未见明显关联。敏感度分析提示Meta分析结果稳定。见表 2。
| 表 2 SMA医院感染暴露因素的Meta分析 Table 2 Meta-analysis on exposure factors of SMA HAI |
|
对各暴露因素指标绘制的倒漏斗图,数据点均匀分布于对称轴两侧,且各部数据点分布于倒漏斗图的中上部,提示无明显发表偏倚。
3 讨论 3.1 医院感染SMA的流行病学特点SMA广泛存在于水、土壤、动物体内,可定植在人和动物的体表和消化道、呼吸道、伤口中,在医院环境、众多医疗设备的污染物、真空采血试管的乙二胺四乙酸抗凝剂、含氯消毒剂以及无菌水中均有分离,感染的科室以ICU为主,其次是呼吸内科和神经内科等[15]。临床上有些病例常发生与其他菌混合感染,其中主要是铜绿假单胞菌、肺炎克雷伯菌、鲍曼不动杆菌,因此,SMA感染治疗困难,病死率高。Muder等[16]报道,SMA菌血症病死率为2l%。Paez等[17]报道,发现SMA感染导致的直接病死率达26.7%,与SMA感染有关的粗病死率在2l%~69%。了解医院感染SMA危险因素,尽早采取针对性的经验治疗,是降低SMA感染死亡的关键。本研究从患者一般情况、合并基础疾病、侵袭性操作及抗菌药物使用情况四个方面对医院感染SMA的暴露因素进行循证医学评价,旨在筛选出SMA感染的危险因素。
3.2 患者一般情况、合并基础疾病与医院感染SMA本研究统计分析的26种暴露因素中有15种是医院感染SMA的危险因素,其中患者入院时一般情况包括APCHE-Ⅱ评分>20分、ICU时间>7 d、住院时间较长和使用糖皮质激素,合并基础疾病主要为免疫缺陷性疾病。APACHE-Ⅱ评分系统是目前国内外应用最广泛的危重病情评估系统,该系统被用于评估患者疾病的严重程度、预后及死亡风险,APACHE-Ⅱ评分越大,说明患者病情越重,预后越差。本研究也提示,SMA感染患者的APACHE-Ⅱ评分高于非SMA感染患者,其中APACHE-Ⅱ评分>20分的合并OR值为3.69。研究[18]报道,APACHE-Ⅱ评分>20分是医院感染多重耐药鲍曼不动杆菌感染的独立危险因素。近年来糖皮质激素在临床滥用趋势较为严重,研究[19-20]报道,长期大剂量使用糖皮质激素是多重耐药菌、真菌感染的高危因素。糖皮质激素具有抑制免疫功能,长期大剂量使用可使患者免疫功能低下,从而增加SMA感染的风险,提示临床应谨慎、合理使用糖皮质激素。患者合并免疫缺陷性疾病是医院感染SMA的危险因素,与免疫缺陷性疾病患者长期服用免疫抑制剂,使免疫功能下降有关。同时,合并COPD、糖尿病、肾功能不全等基础疾病与医院感染SMA无相关性。
3.3 侵袭性操作与医院感染SMA本研究显示,与侵袭性操作相关的危险因素包括机械通气、气管插管、气管切开、中心静脉置管和留置鼻胃管,其中在15种相关危险因素中,机械通气与医院感染SMA的OR值最高(合并OR值为7.59)、其次为气管插管(合并OR值为4.98)、气管切开(合并OR值为4.31),提示机械通气、气管插管和气管切开等侵袭性操作是医院感染SMA的高危因素。侵袭性操作需要突破人体的基础防御屏障,定植于口腔咽喉部的SMA留置导管内壁,容易形成细菌生物膜,增加肺部感染SMA的风险。此外,机械通气等侵袭性操作时间越长,SMA感染的风险也越大。郭立军等[14]报道,有创呼吸机通气时间(>14 d)是医院感染SMA的独立危险因素。因此,提示医务人员应严格掌握侵入性操作的适应证,在操作前、操作中、操作后做到全面评估,若非必需插管,尽量不插管。必需插管时应在病情允许的情况下尽早拔除或者尽量缩短插管的时间[21]。
3.4 抗菌药物用药史与医院感染SMA本研究显示,与抗菌药物使用相关的危险因素包括SMA分离前使用碳青霉烯类药物、含β-内酰胺酶抑制剂药物、氨基糖苷类药物、糖肽类药物及抗菌药物联用品种≥3种。SMA对碳青霉烯类药物天然耐药,2012年中国CHINET嗜麦芽窄食单胞菌耐药性监测显示,除头孢哌酮钠/舒巴坦钠外,SMA对含β-内酰胺酶抑制剂药物的耐药率均超过60%[22]。本研究显示,使用β-内酰胺酶抑制剂与SMA感染相关的合并OR最大(OR=3.52),其次为糖肽类药物(OR=3.42)和碳青霉烯类药物(OR=2.81),提示临床使用此三种药物治疗效果不佳时,应重点关注SMA感染可能。
3.5 本研究局限性(1) 本研究针对所纳入文献的部分影响因素进行合并, 由于部分影响因素如侵入性操作时间, 文献数量有限,无法进行分析。(2)由于不同医疗机构对医院感染的控制力度、重视程度、对抗菌药物使用的监管及侵入性操作的质量控制不同,以及本研究纳入文献发表时间跨度较大,导致危险因素荟萃分析时,出现了一定的异质性。(3)纳入文献中有的未对病例组和对照组的年龄、住院时间等未进行详细区分,故无法进行定量分析。(4)本研究纳入文献的样本量差异较大,可能导致某些因素进行合并分析时出现一定的异质性。(5)仅收集到公开发表的文献,未获得未发表文献,可能会存在一定的发表偏倚。因此,在未来的研究中尚需纳入更大样本进行分析,以提供更加有力的证据支持。
综上所述,本研究显示,入院患者的疾病严重程度、使用糖皮质激素、侵入性操作、广谱抗菌药物及多种抗菌药物联用等均是医院感染SMA的危险因素,临床应采取针对性预防措施,以降低其感染风险。
| [1] |
胡付品, 郭燕, 朱德妹, 等. 2016年中国CHINET细菌耐药性监测[J]. 中国感染与化疗杂志, 2017, 17(5): 481-491. |
| [2] |
熊丽蓉, 冯伟, 向荣凤, 等. 我院2005-2017年嗜麦芽窄食单胞菌的临床分布及耐药性分析[J]. 中国药房, 2018, 29(16): 2248-2251. DOI:10.6039/j.issn.1001-0408.2018.16.19 |
| [3] |
Jeon YD, Jeong WY, Kim MH, et al. Risk factors for mortality in patients with Stenotrophomonas maltophilia bacteremia[J]. Medicine (Baltimore), 2016, 95(31): e4375. DOI:10.1097/MD.0000000000004375 |
| [4] |
Stang A. Critical evaluation of the Newcastle-Ottawa scale for the assessment of the quality of nonrandomized studies in meta-analyses[J]. Eur J Epidemiol, 2010, 25(9): 603-605. DOI:10.1007/s10654-010-9491-z |
| [5] |
Ansari SR, Hanna H, Hachem R, et al. Risk factors for infections with multidrug-resistant Stenotrophomonas maltophilia in patients with cancer[J]. Cancer, 2007, 109(12): 2615-2622. DOI:10.1002/cncr.22705 |
| [6] |
Hottal G, Matsumura M, Kato K, et al. Risk factors and outcomes of Stenotrophomonas maltophilia bacteraemia:a comparison with bacteraemia caused by Pseudomonas aeruginosa and Acinetobacter species[J]. PLoS One, 2014, 9(11): e112208. DOI:10.1371/journal.pone.0112208 |
| [7] |
Nseir S, Di pompeo C, Brisson H, et al. Intensive care unit-acquired Stenotrophomonas maltophilia:incidence, risk factors and outcome[J]. Crit Care, 2006, 10(5): R143. DOI:10.1186/cc5063 |
| [8] |
刘阳, 汤雪萍, 尚学义, 等. 嗜麦芽窄食单胞菌感染危险因素和耐药性分析[J]. 中国消毒学杂志, 2018, 35(4): 258-261. |
| [9] |
吕军, 张昭勇. 嗜麦芽窄食单胞菌医院感染危险因素及预后分析[J]. 湖北医药学院学报, 2014, 33(6): 556-560. |
| [10] |
戴新建, 郑永克, 郑纪阳, 等. 嗜麦芽窄食单胞菌医院获得性肺炎危险因素的探讨[J]. 浙江医学, 2006, 28(5): 392-394. DOI:10.3969/j.issn.1006-2785.2006.05.036 |
| [11] |
查军.医院获得性嗜麦芽窄食单胞菌肺炎细菌耐药性及危险因素分析[D].广州: 广州医科大学, 2015. http://med.wanfangdata.com.cn/Paper/Detail/DegreePaper_D715029
|
| [12] |
石磊, 吴安华, 曹岚, 等. 重症监护病房嗜麦芽窄食单胞菌医院感染的危险因素[J]. 中国感染控制杂志, 2019, 18(5): 403-409. |
| [13] |
许能銮, 石松菁, 赖智双, 等. 重症监护室下呼吸道嗜麦芽窄食单胞菌感染的危险因素分析[J]. 中华结核和呼吸杂志, 2011, 34(10): 735-738. DOI:10.3760/cma.j.issn.1001-0939.2011.10.005 |
| [14] |
郭立军, 李海鹏, 李琼, 等. 神经重症监护室感染嗜麦芽窄食单胞菌的耐药性及危险因素分析[J]. 湘南学院学报(医学版), 2014, 16(3): 21-24. DOI:10.3969/j.issn.1673-498x.2014.03.007 |
| [15] |
叶满, 文晓君. 嗜麦芽窄食单胞菌医院感染和耐药控制[J]. 检验医学与临床, 2011, 8(10): 1238-1239, 1256. DOI:10.3969/j.issn.1672-9455.2011.10.047 |
| [16] |
Muder RR, Harris AP, Muller S, et al. Bacteremia due to Stenotrophomonas (Xanthomonas) maltophilia:a prospective, multicenter study of 91 episode[J]. Clin Infect Dis, 1996, 22(3): 508-512. DOI:10.1093/clinids/22.3.508 |
| [17] |
Paez JI, Costa SF. Risk factors associated with mortality of infections caused by Stenotrophomonas maltophilia:a systema-tic review[J]. J Hosp Infect, 2008, 70(2): 101-108. DOI:10.1016/j.jhin.2008.05.020 |
| [18] |
Wong TH, Tan BH, Ling ML, et al. Multi-resistant Acinetobacter baumannii on a burns unit-clinical risk factors and prognosis[J]. Burns, 2002, 28(4): 349-357. DOI:10.1016/S0305-4179(02)00012-8 |
| [19] |
余悦能, 张祎萍, 金旭红, 等. 肺炎克雷伯菌和大肠埃希菌产超广谱β-内酰胺酶菌株的临床特点及感染的危险因素[J]. 浙江医学, 2016, 38(10): 728-731, 734. |
| [20] |
纪凌云, 周爱萍, 马俊, 等. 白念珠菌唑类药物耐药机制研究进展[J]. 中国感染与化疗杂志, 2019, 19(2): 218-223. |
| [21] |
李娜, 黄艳芳, 唐喻莹, 等. 多重耐药鲍曼不动杆菌医院感染危险因素荟萃分析[J]. 中国感染控制杂志, 2017, 16(2): 115-120. DOI:10.3969/j.issn.1671-9638.2017.02.004 |
| [22] |
艾效曼, 胡云建, 胡志东, 等. 2012年中国CHINET嗜麦芽窄食单胞菌耐药性监测[J]. 中国感染与化疗杂志, 2014, 14(6): 488-492. DOI:10.3969/j.issn.1009-7708.2014.06.006 |



